21世纪经济报道记者 韩利明
近年来,随着大众对医美抗衰需求持续提升,各类新概念医美产品快速走红。
今年3·15晚会上,被冠以“抗衰界宠儿”的“外泌体”产品被集中曝光——这类产品在市场上被包装为兼具美容抗衰与疾病治疗功效的“万能神药”,售价高昂,成为医美领域热度最高的品类之一。
央视调查显示,外泌体是干细胞培养过程中分泌的生物活性物质,在医疗界和学术界,其作用机理、临床测试等多项医学程序上,尚不能明确,更多还停留在学术研究和理论研究的阶段。
2025年6月,国家药品监督管理局药品审评中心已发布征求意见稿,将具有治疗功能、依靠活性成分发挥作用的外泌体,纳入药品监管。截至目前,我国尚无外泌体药品获得上市销售批准,行业监管仍在进一步完善中。
那么,当前外泌体领域有哪些企业布局?科研端与产业端真实进展如何?
多家企业紧急发布声明
据央视新闻曝光,网络平台流传的营销视频中,这些未获国家相关批准的“外泌体抗衰”产品,竟被标称“第二类医疗器械”,被各类医美机构用于美容抗衰项目,且定价居高不下。
但事实上,目前我国并没有允许以外泌体为成分的医疗器械产品上市销售。其中,生产商灏麟(天津)生物科技有限公司的工作人员直言,目前医疗器械证分类中并无“外泌体”这一类别,该公司生产的外泌体产品,为规避市场监管,违规套用了胶原蛋白的医疗器械许可证。
3月16日上午,北交所“重组胶原蛋白第一股”锦波生物官微发布声明,明确指出“3・15”晚会报道的某生物科技有限公司生产的“轻澄”等产品,系套用人源化胶原蛋白二类医疗器械许可证,违规添加外泌体成分。
锦波生物方面强调,此类“套证”行为,不仅严重违反《医疗器械监督管理条例》,更将未经安全性验证的物质直接用于人体注射,置消费者健康于不顾。同时,这种恶意套用合法产品注册证的行为,严重扰乱市场秩序,损害了合规人源化胶原蛋白企业的声誉。
“根据国家药品监督管理局的规定,凡是注入人体真皮组织或血液循环的医疗器械,均属于风险程度最高的三类医疗器械,必须通过严格的药学研究、临床试验和审评审批,取得‘械注准3’注册证后方可上市使用。二类医疗器械仅适用于非侵入性或浅表性使用,绝不可用于注射。”锦波生物方面进一步指出。
套证生产、违规添加、违规销售,仅仅是外泌体医美乱象的冰山一角。市场上还有部分企业开展虚假宣传,称其能治疗多种疾病。由于此类企业大多不具备医疗资质,所以外泌体注射只能找医疗机构进行合作,业内将这种操作方式称为“借台代打”。
这些既无国家批准、未通过任何临床试验,也无任何疗效数据支撑的所谓“外泌体”产品,背后却暗藏巨额利润。据介绍,“第一次用1500亿颗粒数,第二次用2000亿颗粒数,第三次用2500亿颗粒数。这样循序渐进,总共用6000亿颗粒数,向顾客收6万元。”
乱象之下,消费者投诉与吐槽频发。网络上充斥着大量关于“外泌体抗衰”的负面反馈:“我就做了外泌体,结果全脸感染,长出严重痤疮”“我打了之后过敏,烂脸三个月都没好”“几乎毫无效果,纯粹是骗钱的”......
随着3·15晚会点名外泌体医美乱象,相关平台也迅速做出整改。有资料显示,新氧安心美小程序曾有乔洛施AR外泌体项目在售,并导流至线下医美机构。对此,新氧方面已明确表示,目前所有外泌体相关项目均已下架。
科研端、产业界进展如何?
事实上,全球范围内,有关外泌体的违规乱象也多有发生。
美国食品药品监督管理局(FDA)曾在2019年发布通知显示,内布拉斯加州有患者使用未经批准、标榜含有外泌体的产品后出现严重不良事件。FDA提醒,用于治疗人类疾病和相关状况的外泌体,属于药物和生物制品范畴,需接受相关监管,并满足上市前审查和批准要求。但有部分诊所向患者提供外泌体产品,声称这些产品有潜力预防、治疗或治愈各种疾病或状况。
尽管乱象频发,但外泌体本身的科研价值不可忽视。根据公开资料,外泌体(exosome)作为一种来源于细胞的天然纳米囊泡,因其独特的细胞间通讯功能与分子递送能力,正逐渐成为连接生物治疗与药物递送技术的重要桥梁,并受到全球生物医药领域的广泛关注。
Brainstorm Cell公司总裁兼首席医学官Ralph Kern博士曾公开分享,“在不同的神经退行性疾病、眼部疾病、视网膜疾病,甚至急性呼吸窘迫综合征(ARDS)中进行的研究证明,利用外泌体靶向递送药物的优势,在减少组织损伤和减少炎症方面,对靶组织都有深远的影响。”
不过21世纪经济报道记者从多位业内人士处获悉,目前全球范围内尚未有获批上市的外泌体治疗性药物,相关开发工作停留在实验室和临床试验阶段。一方面,外泌体研究和商业化应用涉及合规风险,产生外泌体的人源性细胞来源合法性问题是其中关键。另一方面,外泌体的质量难以保证。深圳科诺医学检验实验室日前也发布文章显示,外泌体制剂或细胞外囊泡的质量分析方法,至今仍是全球性的难题。
2024年发表于《Clinical and Translational Science》期刊的一篇文章显示,一款基于外泌体的治疗药物,需在明确其分子组成与结构,并证明其药代动力学特征及治疗有效性后,方可获得临床批准。但对外泌体的药代动力学与治疗有效性进行验证,对监管机构而言仍具有挑战性。
尽管存在诸多瓶颈,科研端与产业界对外泌体的探索从停止。根据医药魔方数据,目前全球范围内有293款外泌体创新药。
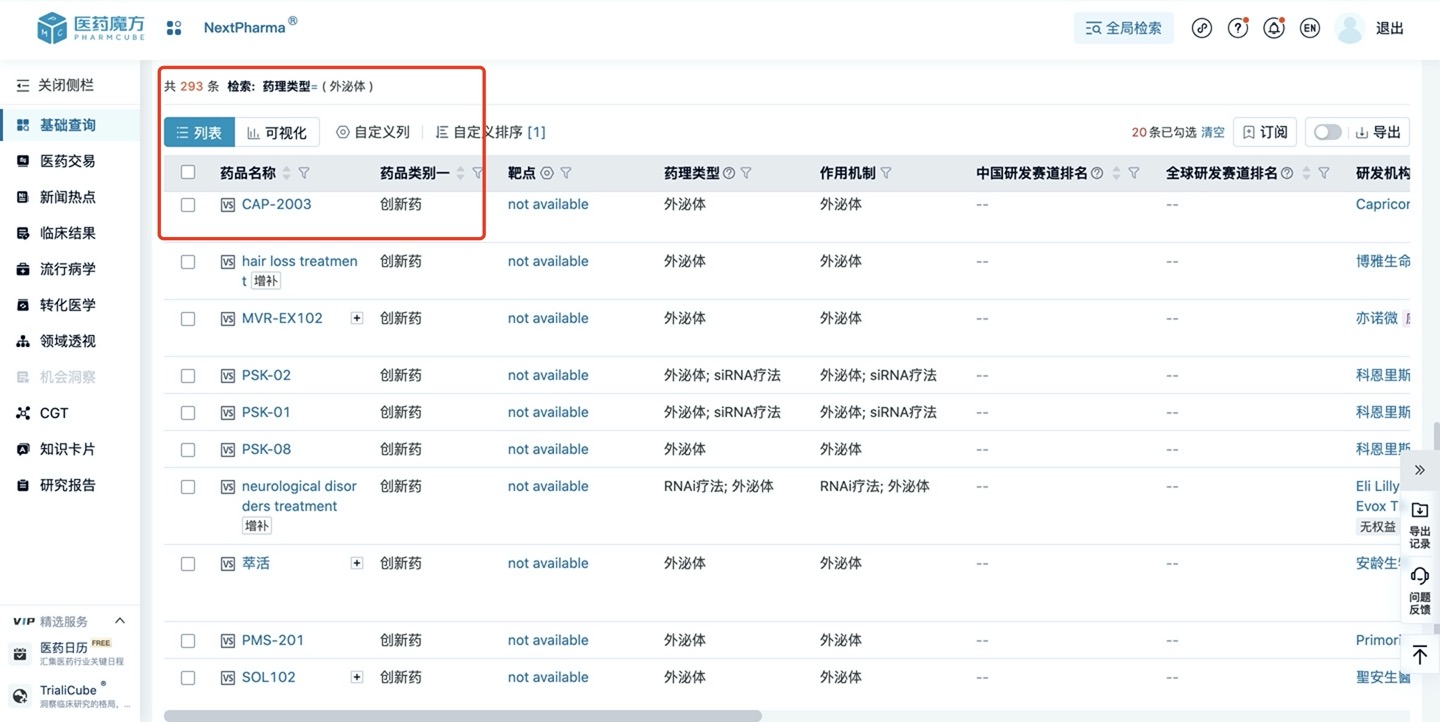 图片来源:医药魔方
图片来源:医药魔方
公开资料显示,2026年3月10日,专注于开发罕见病转化性细胞和外泌体疗法的Capricor Therapeutics宣布,美国FDA已撤销此前发布的《完整回复函》(Complete Response Letter,CRL,通常用以列明相关缺陷并给出整改建议),并恢复对其生物制剂许可申请(“BLA”)的审查,该申请旨在全面批准Deramiocel。
据悉,Deramiocel(CAP‑1002)由异体心球来源细胞(CDCs)构成,这类罕见心脏细胞在临床前与临床研究中已被证实,在杜氏肌营养不良(DMD)等肌营养不良症中,可通过强效免疫调节与抗纤维化作用,保护心脏及骨骼肌功能。CDCs 通过分泌一类被称为外泌体的细胞外囊泡发挥作用:外泌体可靶向巨噬细胞,并改变其表达谱,使其向修复型表型转化,而非促炎表型。
在我国,也有不少企业布局外泌体领域。例如科兴制药在2025年9月公告称,在研的外泌体原料近日已正式通过美国FDA的II型药物主文件(DMF)备案(备案号:042265),这一成果不仅标志着公司外泌体技术达到国际权威标准,也将为公司在外泌体领域的全球化布局奠定基础。
此外,恩泽康泰官微日前也发布消息显示,欧莱雅集团的研发与创新中心在国际知名期刊《Frontiers in Cell and Developmental Biology》上发表了一项关于皮肤抗衰老的突破性原创研究论文,首次在3D全层重建皮肤模型中,深入探讨了干细胞外泌体(学名细胞外囊泡,EVs)在皮肤再生和抗衰老过程中的显著作用。在这项研究中,使用的干细胞外泌体产品以及miRNA测序服务,均由恩泽康泰提供。
有业内人士向21世纪经济报道记者表示,当前市场上对外泌体的营销与炒作已产生了负面效应,“这种乱象或许会让公众对这一具有潜力的治疗方向产生更多误解和抗拒,让外泌体领域的发展道路更加曲折,不利于行业的长期健康发展。”
该人士同时强调,外泌体等前沿技术的发展离不开规范监管,“随着今年生物医药在政府工作报告中被提升至支柱性产业的高度,加之3·15晚会同步点名多款健康领域违规产品,这一趋势令人欣喜——行业越规范,越能实现良性可持续发展,也体现出国家对生物医药行业的重视程度不断提升。”
















